
引言:
抗体偶联药物(ADCs)在肿瘤靶向治疗中取得了巨大成功,但其在实体瘤中的疗效常受限于较差的肿瘤组织穿透性:传统ADC庞大的分子量(~150 kDa)和强二价结合力构成了严重的屏障,导致其难以穿透血管并深入肿瘤实质。为解决这一问题,研究人员尝试开发分子量更小的抗体片段-药物偶联物(FDCs,13-50 kDa)以增强穿透力,但这却不可避免地导致药物在血液循环中被快速肾脏清除,半衰期极短,极大削弱了其治疗潜力。

为了打破这一临床僵局,2026年4月29日,夜色直播-夜色直播app-夜色直播下载 天然药物及仿生药物全国重点实验室刘涛教授、王永副研究员团队在Journal of Medicinal Chemistry杂志上发表了题为“Tumor Microenvironment-Responsive Antibody Fragment-Cleavable PEGylated Drug Conjugates (AFCDC) for Improved Tumor Penetration and Antitumor Efficacy”的研究论文。该研究创新性地提出了一种肿瘤微环境响应型抗体片段-可裂解PEG化药物偶联物(AFCDC)平台,通过基因编码的非天然氨基酸(ncAA)实现了双功能定点修饰,成功解决了抗体片段药物在实体瘤治疗中“穿透力”与“半衰期”无法兼顾的难题,为下一代实体瘤靶向治疗提供了极具潜力的新型递送策略。
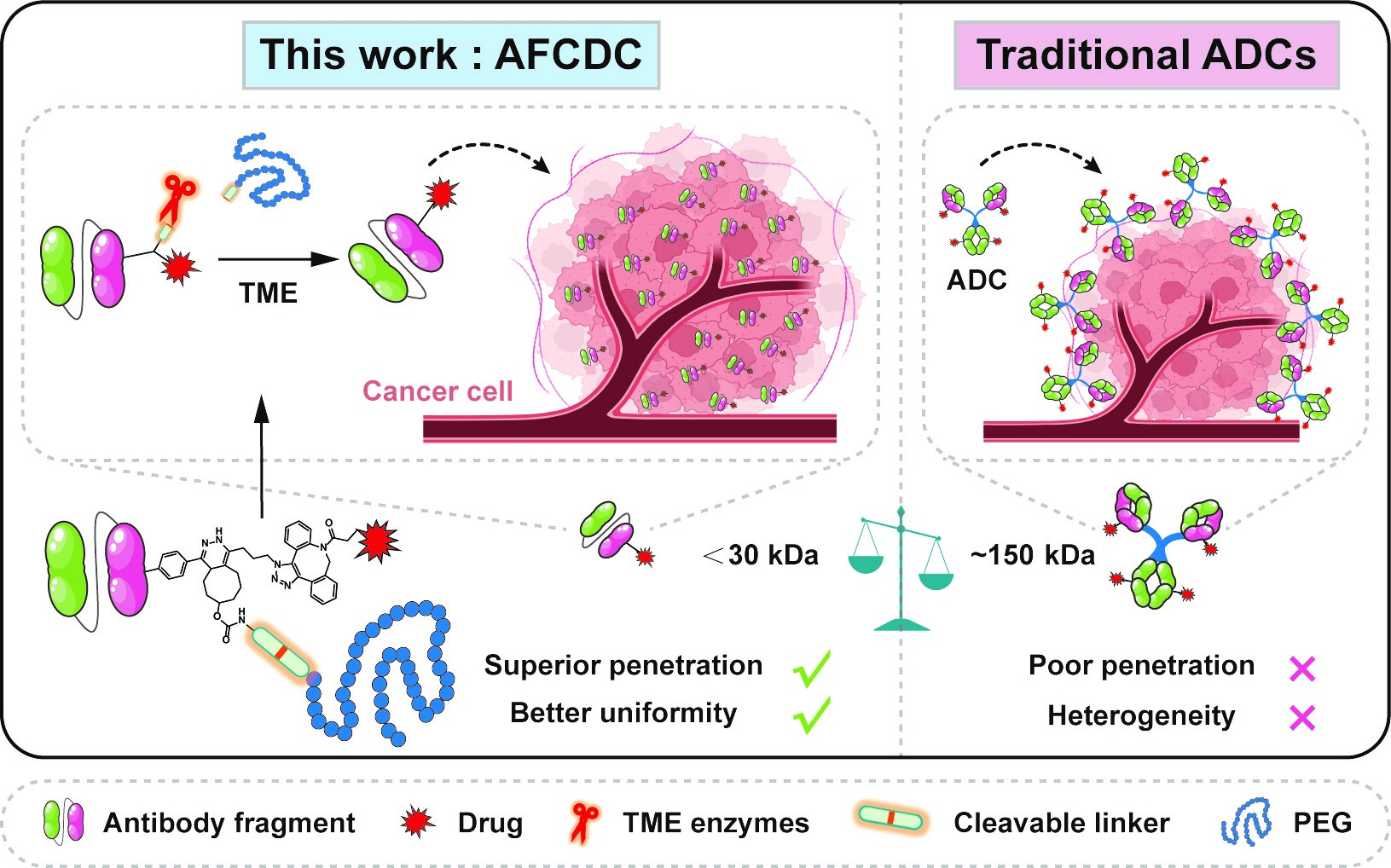
该AFCDC平台利用含有双功能基团的非天然氨基酸(pTAF),在单链抗体(scFv)核心上实现了细胞毒素与基质金属蛋白酶2(MMP2)可裂解的聚乙二醇(PEG)链的精准双定点偶联。这一设计赋予了分子“智能”的体型调节能力:在血液循环中,大分子PEG链可显著延长药物半衰期;而当药物抵达高表达MMP2的肿瘤微环境时,PEG链被特异性酶切脱落,实现分子尺寸从大到小的转变,恢复抗体片段原有的紧凑结构,从而以极强的穿透力将毒素带入肿瘤深部杀伤癌细胞。
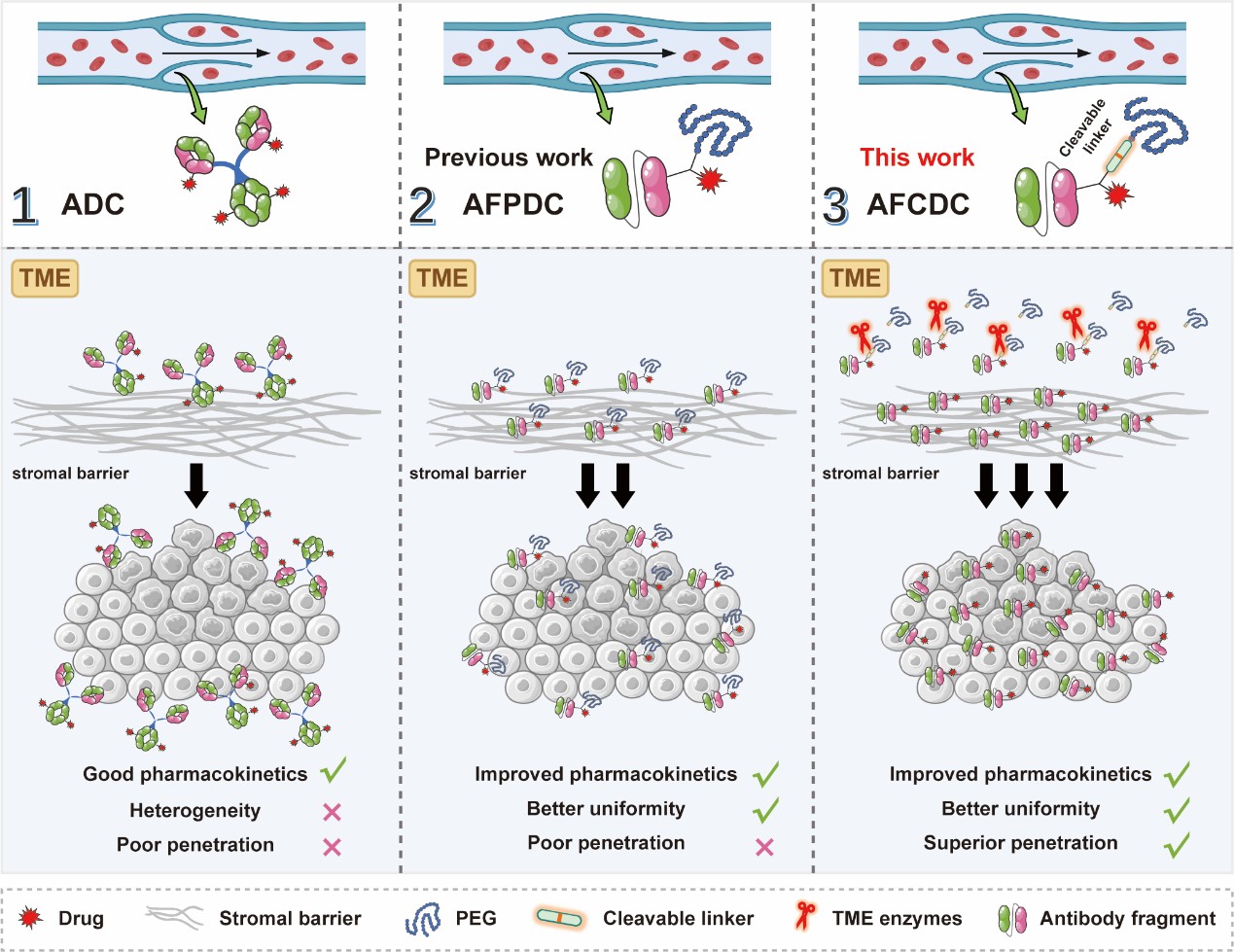
图1. AFCDC的迭代升级与作用机制
研究内容
肿瘤微环境响应连接子的合成与穿透力验证
研究团队首先通过多肽固相合成技术构建了包含MMP2特异性酶切序列的PEG衍生物,并利用正交点击化学反应,将其与荧光探针或毒素分子精准偶联至scFv的特定位点。在穿透力评估实验中,研究人员采用了红色荧光Cy5探针来追踪药物的分布。离体与活体实验均有力证实,在MMP2酶的作用下,脱除PEG的AFCDC向实体瘤深处的渗透能力获得了大幅提升;在肿瘤核心区域内AFCDC的红色荧光信号达到了非裂解对照组的6倍以上,展现出显著的穿透提升。
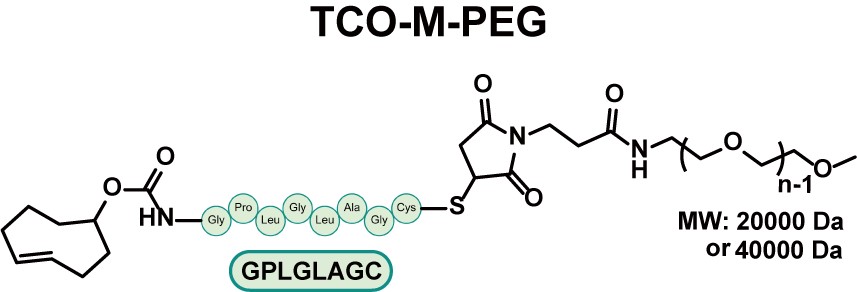
图2. TME响应连接子的构建
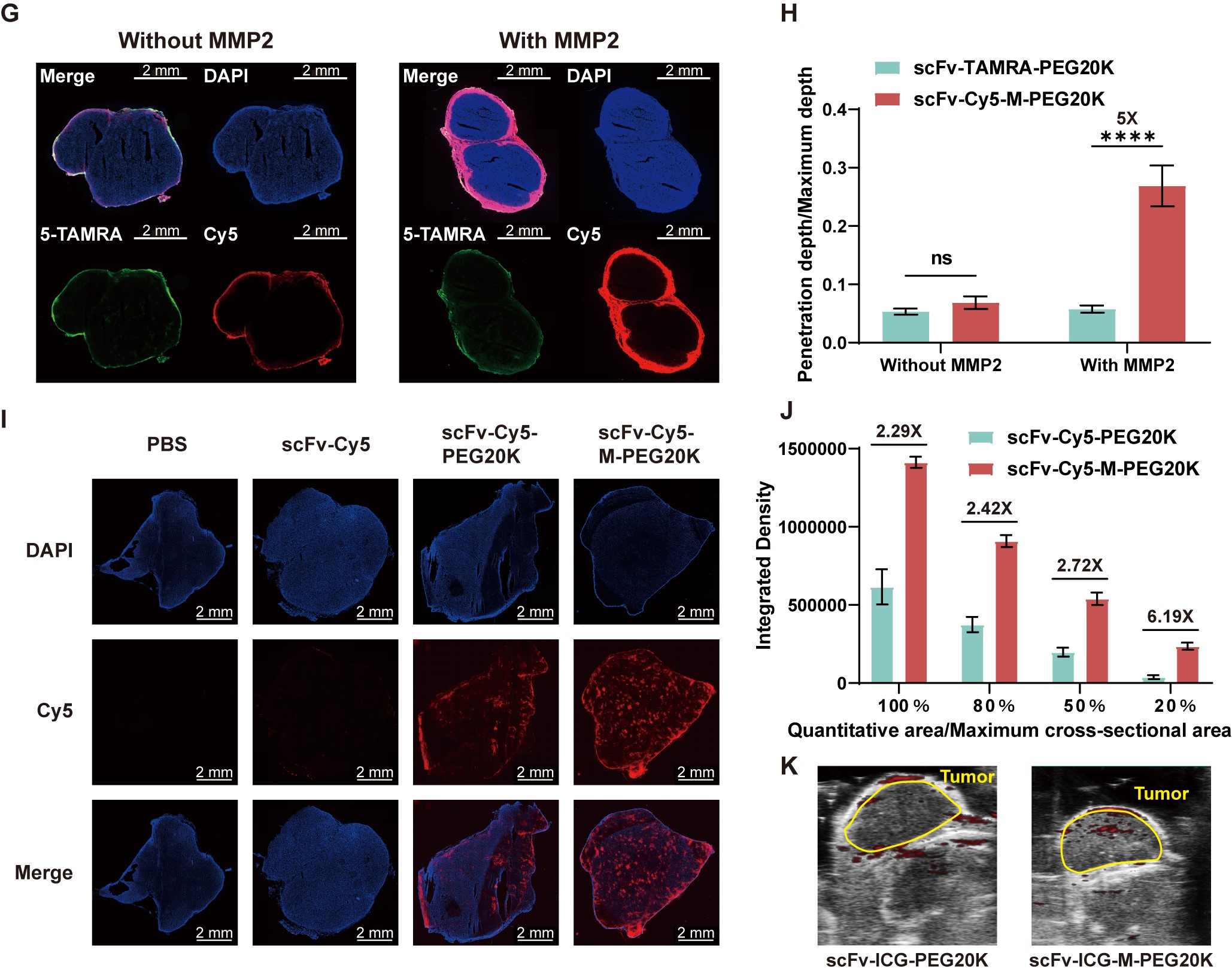
图3. AFCDC的肿瘤穿透力验证
SK-OV-3肿瘤模型中的长效药代动力学与药效评价
在HER2阳性卵巢癌(SK-OV-3)模型中,研究者验证了PEG化对药物半衰期的关键作用。药代动力学数据显示,AFCDC的消除半衰期达到了21.35小时,远超未修饰片段的1.6小时,保障了药物在体内的长效循环。在体内药效评价中,AFCDC组显著抑制了肿瘤的生长,其生存期与抑瘤率均明显优于不可裂解的AFPDC,且小鼠体重维持平稳,证明了该体系通过“尺寸重塑”卸载PEG后,不仅打得深,而且安全性极佳。
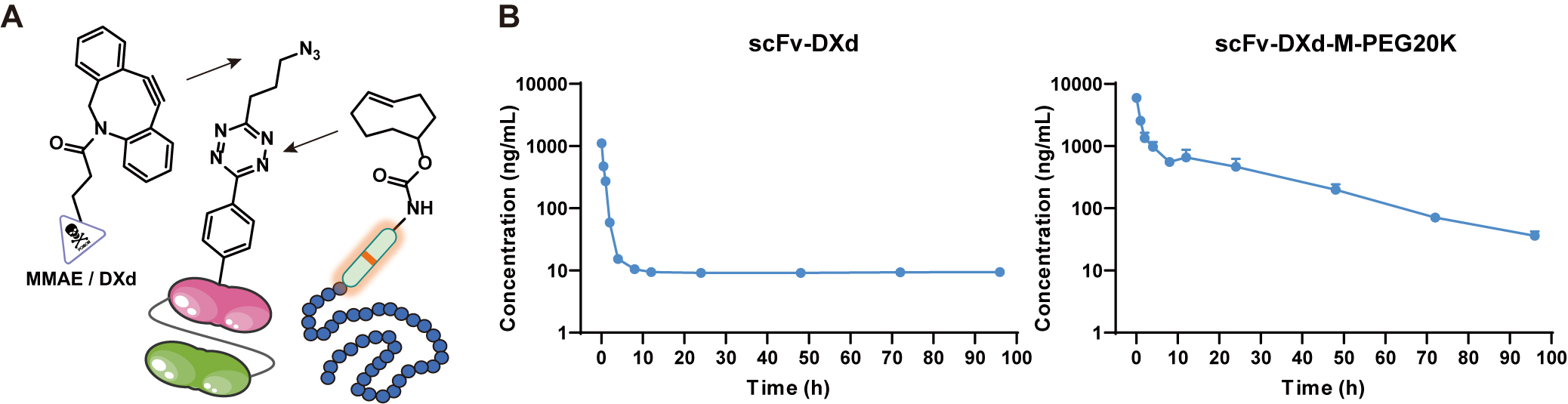
图4. 药代动力学评价
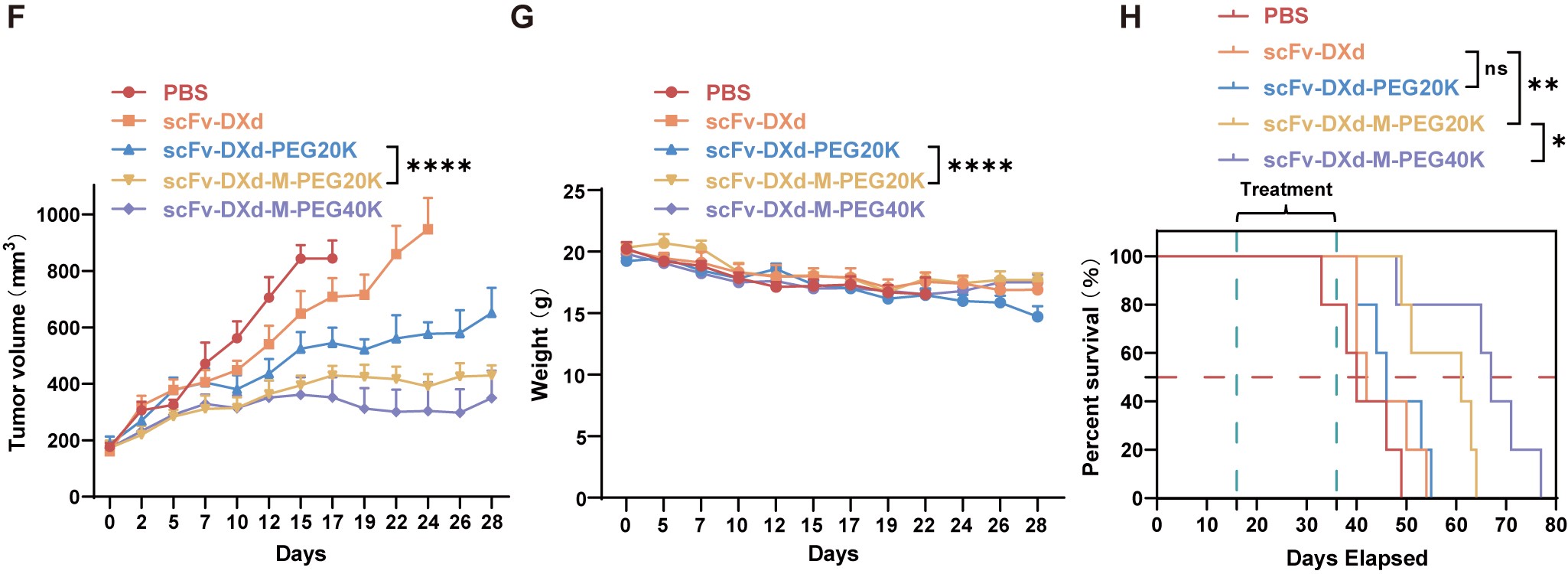
图5. 卵巢癌小鼠模型上药效评价
在NCI-N87模型中与临床ADC金标准对比
为了进一步评估AFCDC在临床转化中的竞争潜力,团队在NCI-N87胃癌异种移植模型中进行了深入测试。结果显示,AFCDC的抑瘤效果呈现出良好的剂量依赖性,且在10 mg/kg剂量下的抗肿瘤活性显著优于非响应型对照组。值得注意的是,在与临床获批药物Enhertu ®(T-DXd)的药效对比实验中,在各自优化适宜的给药方案下,AFCDC疗效显著超越了标准的4mg/kg T-DXd组,诱导了肿瘤的近乎完全消退。
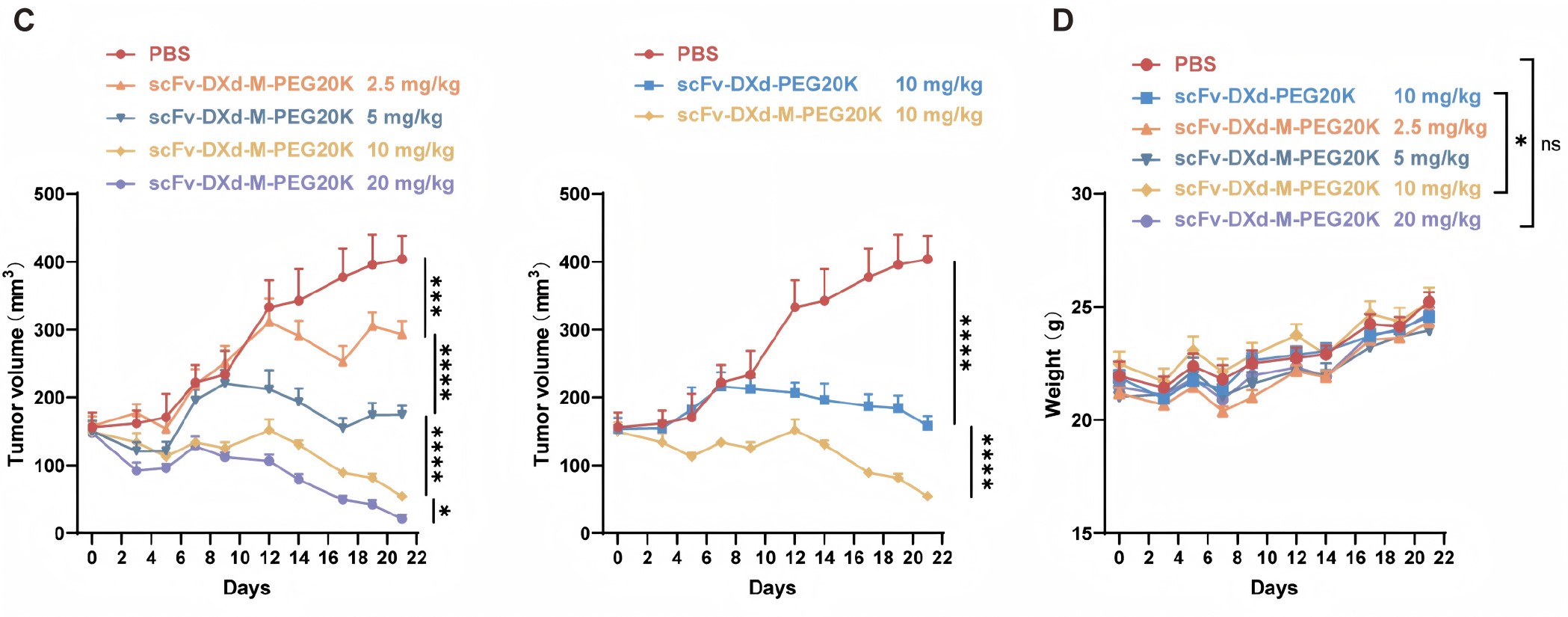
图6. 胃癌小鼠模型上药效剂量依赖性评价
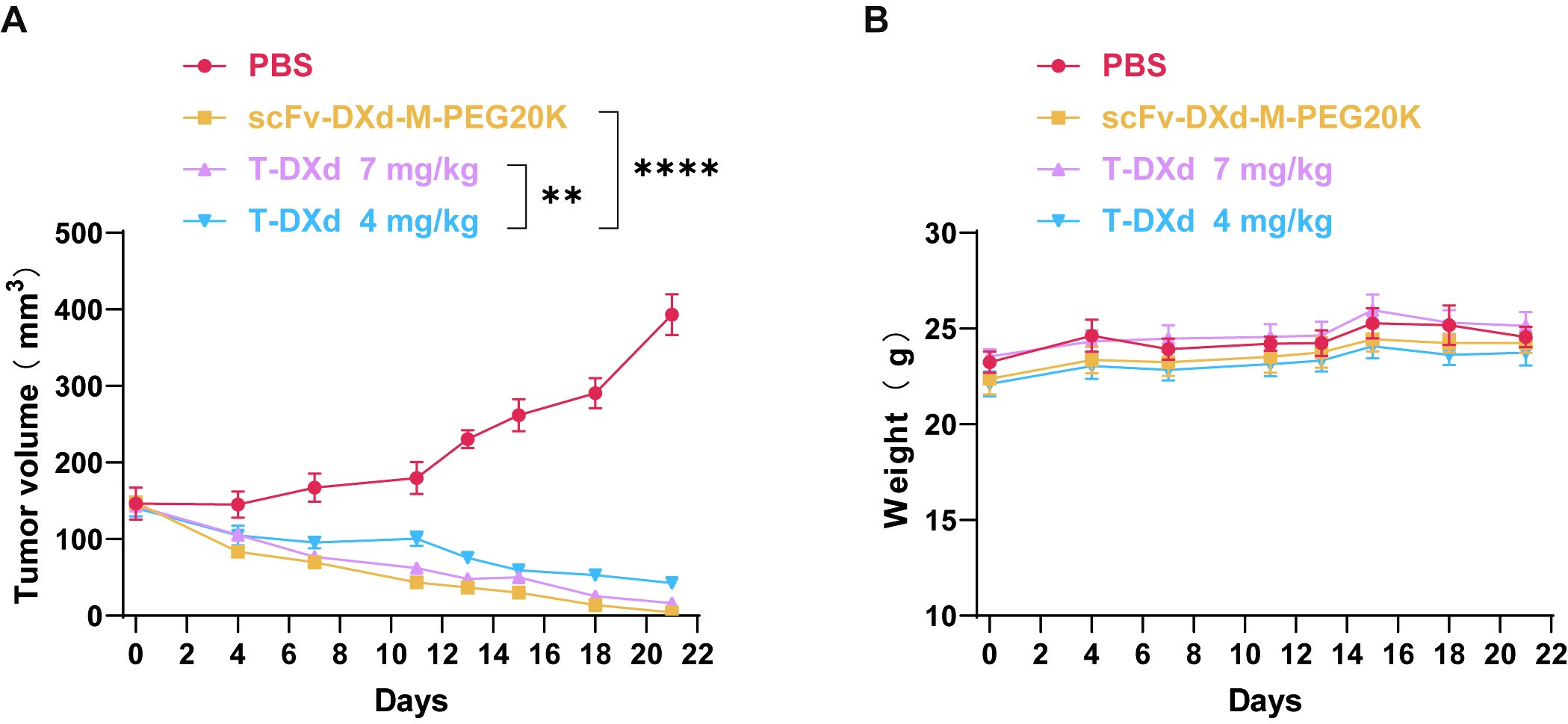
图7. 与临床金标准ADC进行药效对比
平台模块化拓展:针对B7-H3靶点的纳米抗体深度应用
为证明AFCDC平台具有普适的模块化开发能力,研究人员将核心抗体替换为针对另一热门实体瘤靶点——B7-H3的纳米抗体。通过精确的结构分析与位点筛选,团队成功将pTAF引入纳米抗体的非CDR区域(N88位点),并装载了DXd毒素与PEG40K链。内吞实验与体内药效学验证再次确证,这种基于纳米抗体的新型AFCDC同样能在小鼠模型中展现出强劲且安全的抗肿瘤疗效,这充分证明了该“智能解体”策略不仅适用于scFv,还能广泛兼容各类新颖的微型蛋白质骨架。
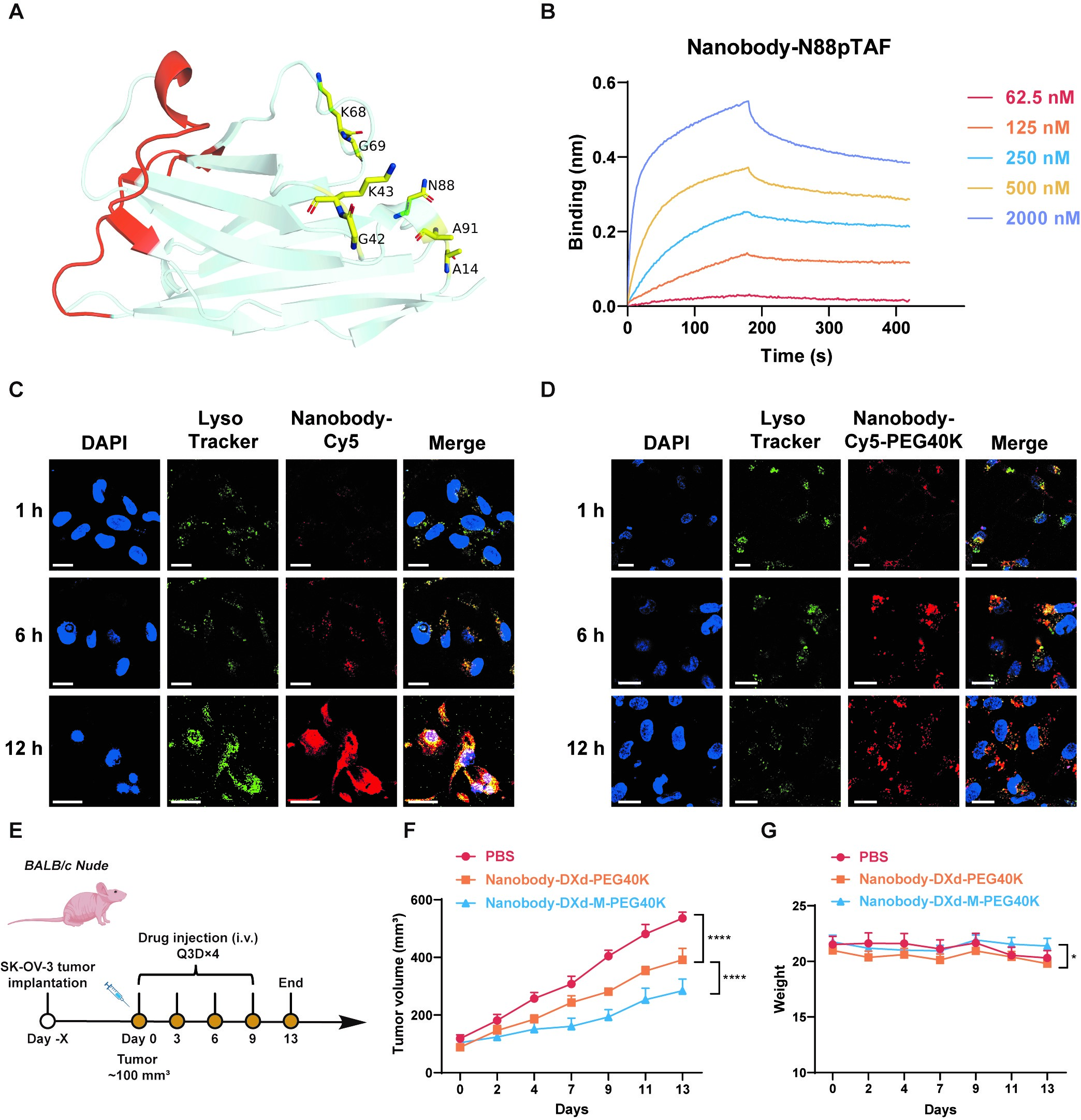
图8. 在B7-H3纳米抗体上验证AFCDC普适性
总结:
该研究提出并验证了肿瘤微环境响应型AFCDC平台。通过精准的基因密码子扩展技术与正交化学修饰,AFCDC成功打破了抗体片段在“肿瘤穿透力”与“全身半衰期”之间的长期矛盾。这种肿瘤微环境尺寸动态重塑策略,不仅为HER2阳性实体瘤提供了极具竞争力的靶向治疗方案,其高度模块化的特性也为未来搭配不同靶点、不同毒素及多种微环境触发机制奠定了坚实的基础,为新一代高效实体瘤ADC的开发指明了科学路径。
夜色直播-夜色直播app-夜色直播下载 刘涛教授和王永副研究员为该研究论文的共同通讯作者。夜色直播-夜色直播app-夜色直播下载 2022级博士研究生王昕为论文的第一作者,团队成员侯晓宇、谭琳致、陈灿璞、常丽颖、韩伯阳、邢韵奇、曾志英、周子婷、路强、谢乐怡、陆梓仪、赵恪锐、曹宝山教授为该研究做出了重要贡献。该研究得到了中国国家重点研发计划、国家自然科学基金以及北京市自然科学基金的大力支持。
论文链接: //doi.org/10.1021/acs.jmedchem.5c03215
通讯作者简介:

刘涛,北京大学博雅特聘教授,国家杰青、国家优青、北京市杰青基金获得者,夜色直播-夜色直播app-夜色直播下载 分子与细胞药理学系主任。担任ACS Omega杂志副主编和Journal of Molecular Biology杂志编委,任中国医药生物技术协会合成生物学分会委员、中国生物工程学会合成生物学分会青年工作组委员。获中国药学会生物医药青年奖、拜耳学者奖、屠呦呦青年学者奖、北京大学王选青年学者奖等。以通讯作者身份在Nat. Chem., Nat. Chem. Biol., Mol. Cell, Nat. Commun., Sci. Adv., Chem, JACS, ACIE, Chem. Rev.等上发表论文30余篇。研究集中在基于细胞工程的蛋白质精准化学修饰技术,通过非天然氨基酸介导的蛋白质化学修饰实现蛋白质、病毒以及细胞等生物技术药物的升级换代与创新。

王永,北京大学副研究员。以第一( 含共同)/ 通讯( 含共同) 作者身份在Nat. Commun., Angew. Chem. Int. Ed., Adv. Sci., J. Med. Chem., Nano Lett., Bioorg. Med. Chem., Methods Mol. Biol.等发表论文多篇。主要研究方向为基于生物合成的蛋白质遗传编码与蛋白质的精准化学修饰,致力于构建新型生物正交反应工具,推动蛋白质药物的功能优化与创新应用,研究内容聚焦于抗体-药物偶联(ADC) 和细菌治疗等领域。
第一作者简介:

王昕,夜色直播-夜色直播app-夜色直播下载 化学生物学专业2022级博士研究生,研究兴趣为新型抗体偶联药物的开发。在学期间以第一作者或共同作者身份在J. Med. Chem., Eur. J. Med. Chem., Angew. Chem. Int. Ed., J. Am. Chem. Soc., Nat. Comm.等杂志上发表多篇学术论文。
天然药物及仿生药物全国重点实验室