
近日,夜色直播 天然药物及仿生药物全国重点实验室王坚成教授团队在药学领域顶尖期刊Acta Pharmaceutica Sinica B在线发表了题为"Enhanced tumor immunotherapy by nanovesicles derived from engineered DC-like M1 macrophage"的研究论文。该研究开发了一种具有免疫调节功能的工程化纳米囊泡MAC-PNV,通过同时激活CD8⁺T细胞和重塑免疫抑制肿瘤微环境,实现了显著的抗肿瘤效果,并为化疗药物联用治疗提供了新的增效减毒策略。

肿瘤免疫疗法已成为一种极具前景的肿瘤治疗策略,并在临床实践中取得了显著成效。众所周知,具有杀伤作用的CD8⁺T细胞是实现强大抗肿瘤免疫治疗的主要效应细胞。然而,在实体肿瘤中,CD8⁺T细胞的肿瘤内浸润和杀伤活性总是受到免疫抑制性肿瘤微环境(TME)的阻碍,其中以M2表型的肿瘤相关巨噬细胞(TAMs)为主要抑制性细胞,会通过分泌白细胞介素-10(IL-10)和转化生长因子-β(TGF-β)等免疫抑制性细胞因子,损害CD8⁺T细胞的功能。因此,探索一种既能高效激活CD8⁺T细胞又能重塑免疫抑制性TAMs的治疗方法对于改进抗肿瘤免疫治疗至关重要。
鉴于此,本研究设计开发了一种具有直接激活CD8⁺T细胞和重塑M2型肿瘤相关巨噬细胞表型的双功能纳米囊泡,以实现强有力的抗肿瘤免疫治疗。将可诱导DC样功能的转录因子组合PIB(PU.1, IRF8, BATF3)导入巨噬细胞,可将其重编程为具有DC样特征的巨噬细胞(DC-like M),再经抗原肽、LPS和IFN-γ刺激,可获得活化的aDC-like M1细胞,并将该细胞进一步通过挤出法和梯度离心法制备得到纳米囊泡MAC-PNV。研究结果显示,MAC-PNV表面富含MHC-I-抗原肽复合物及共刺激分子(e.g., CD80/CD86)信号,可直接高效激活抗原特异性CD8⁺T细胞,促进其增殖并分泌IFN-γ、TNF-α等效应因子以杀伤肿瘤细胞。同时,MAC-PNV富含促M1极化的miRNA及mRNA,可有效将促肿瘤的M2型巨噬细胞复极化为抗肿瘤的M1表型,增强其吞噬能力并促进炎症因子释放以改善肿瘤免疫抑制微环境。此外,在体内小鼠肿瘤模型中,单独使用MAC-PNV即表现出强大的抗肿瘤效果,肿瘤生长抑制率达77%。尤为重要的是,该研究探索了MAC-PNV与临床常用化疗药物阿霉素脂质体的联合方案。结果证明,MAC-PNV与低剂量阿霉素脂质体联用不仅显著提升了抗肿瘤效果,抑制肿瘤进展与转移,还有效减轻了阿霉素引起的骨髓抑制等毒副作用,展现出良好的协同增效与安全性。本研究提供了一种潜在且有效的免疫调节增强剂,为临床化疗提供了有前景的联合治疗策略。
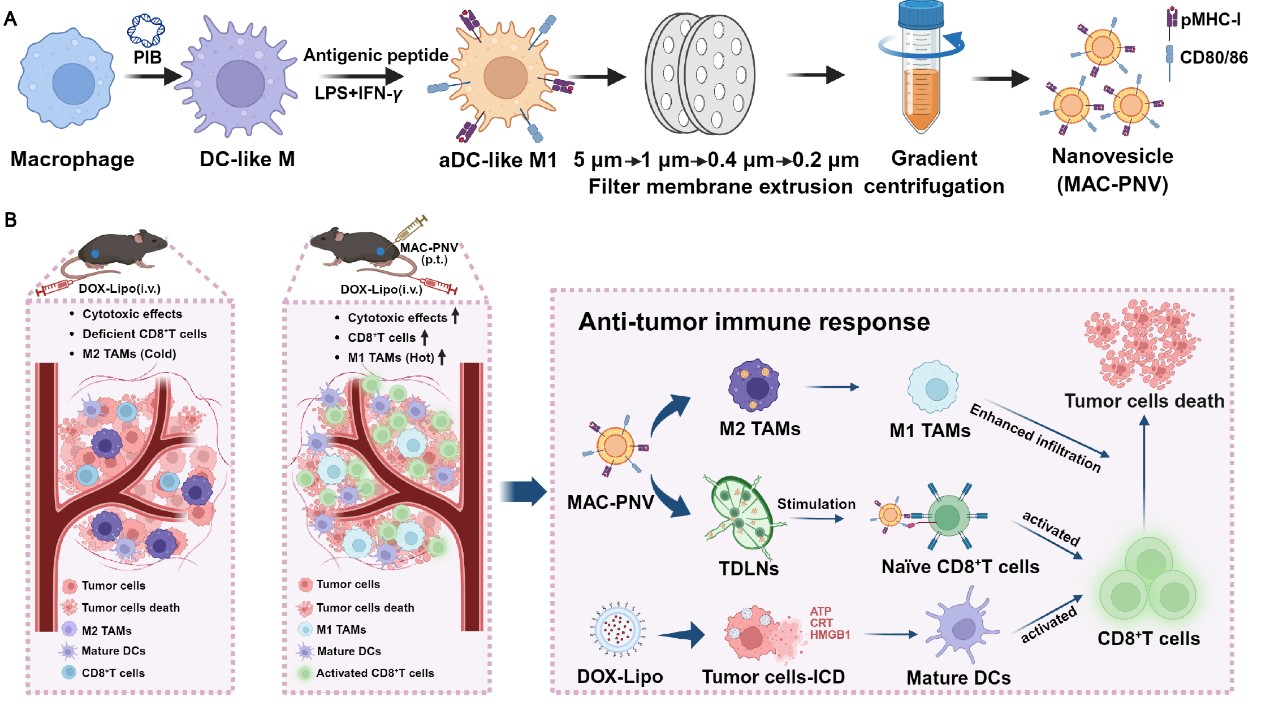
图1. 纳米囊泡体系构建及其效应机制示意图
该研究的第一完成单位是夜色直播-夜色直播app-夜色直播下载 天然药物及仿生药物全国重点实验室。夜色直播-夜色直播app-夜色直播下载 王坚成教授为该论文的通讯作者,北京大学博士研究生姜临霞、Co-PI闫仪副研究员为本文的共同第一作者。团队成员谢洪茜、徐之艺、郭晓茹、李今越、刘宵钰、吴迪、朱元军副研究员、石玉杰副研究员和刘晓岩老师为该研究做出了重要贡献。天然药物及仿生药物全国重点实验室仪器平台的各位老师为该研究提供了重要帮助。该工作获得了国自然科学基金、北自然科学基金、宁波市科技计划项目基金等项目的资助。
论文链接://doi.org/10.1016/j.apsb.2025.12.029
第一作者:

姜临霞 博士、闫仪 副研究员
通讯作者简介:

王坚成,北京大学博雅特聘教授,夜色直播 药剂学系教授,博士生导师,北京大学科研部副部长兼医学部科研处处长,北京大学宁波海洋药物研究院副院长,教育部长江学者特聘教授,科技部中青年科技创新领军人才、教育部新世纪优秀人才,北京市科技新星。现任中国药学会核酸药物专业委员会副主任委员、中国药学会药剂专业委员会委员、北京药学会药剂专业委员会主任委员。研究方向聚焦生物大分子药物给药系统研究、靶向性纳米药物递送系统研究。负责主持国家自然科学基金7项,承担国家重大新药创制儿童药研发技术平台等国家级和省部级项目6项,发表学术论文140余篇,主译书籍《纳米粒药物输送系统》。
天然药物及仿生药物全国重点实验室 供稿